![]()
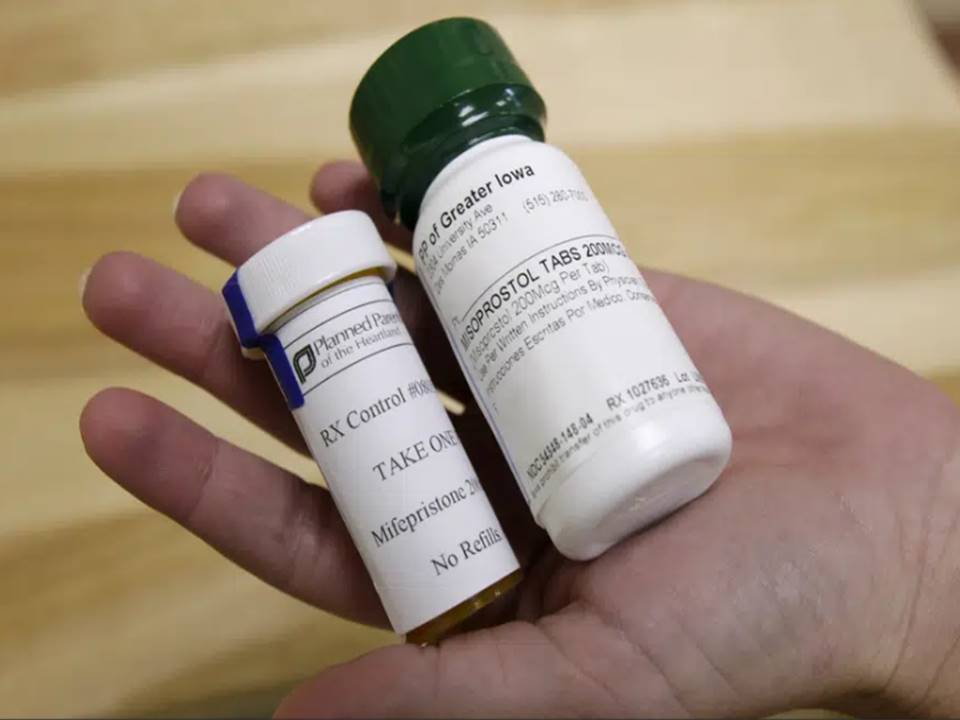
Una corte federal de apelaciones dictaminó que la píldora abortiva mifepristona todavía se puede usar por ahora, pero redujo el período de embarazo en el que se puede tomar el medicamento y dijo que no se podía entregar por correo.
La decisión redujo temporalmente un fallo de un juez de primera instancia en Texas que había bloqueado por completo la aprobación por parte de la Administración de Drogas y Alimentos del método de aborto más utilizado en la nación.
Aun así, evitar que la píldora se envíe por correo equivale a otra restricción significativa del acceso al aborto: menos de un año después de que la reversión de Roe v. Wade resultó en que más de una docena de estados prohibieran el aborto por completo.
Es probable que el caso llegue a la Corte Suprema de EE.UU.
“Vamos a seguir luchando en los tribunales, creemos que la ley está de nuestro lado y prevaleceremos”, dijo el jueves la secretaria de prensa de la Casa Blanca, Karine Jean-Pierre, hablando con periodistas desde Dublín durante una visita del presidente Joe Biden.
Los opositores que entablaron la demanda de Texas contra la droga el año pasado calificaron la decisión de la Corte de Apelaciones del Quinto Circuito de EE. UU. como una victoria.
La mifepristona fue aprobada por la FDA hace más de dos décadas y se usa en combinación con un segundo fármaco, el misoprostol.
Los grupos de derechos del aborto expresaron su alivio de que la aprobación de la FDA se mantuviera vigente por ahora, pero criticaron a la corte por restablecer las restricciones sobre el medicamento.
Whole Woman’s Health, un proveedor de servicios de aborto que opera seis clínicas en cinco estados, dijo en un tuit que continuarían ofreciendo mifepristona en las clínicas y a través de servicios virtuales mientras revisaba la decisión.
En la votación de 2-1, el panel de jueces suspendió los cambios realizados por el regulador desde 2016 que relajaron las reglas para recetar y dispensar mifepristona. Entre ellas, extender el período de embarazo en el que se puede usar el medicamento de siete a 10 semanas, y también permitir que se dispense por correo, sin necesidad de visitar un consultorio médico.
La demanda que desafía la aprobación del fármaco fue presentada por Alliance Defending Freedom, que también estuvo involucrada en el caso que anuló Roe v. Wade.
“La decisión del Quinto Circuito es una victoria significativa para los médicos que representamos, la salud de la mujer y todos los estadounidenses que merecen un gobierno federal responsable que actúe dentro de los límites de la ley”, dijo Erin Hawley, abogada del grupo.
Los dos jueces que votaron para endurecer las restricciones, Kurt Engelhardt y Andrew Oldham, son designados por el expresidente Donald Trump. La tercera jueza, Catharina Haynes, es una persona designada por el ex presidente George W. Bush. Ella dijo que habría suspendido por completo el fallo del tribunal inferior por ahora para permitir los argumentos orales en el caso.
Los jueces de la corte de apelaciones, en su mayoría, señalaron que la administración Biden y el fabricante de mifepristona “nos advierten de las consecuencias públicas significativas” que resultarían si la mifepristona se retirara por completo del mercado según el fallo del tribunal inferior.
Pero los jueces sugirieron que los cambios de la FDA que facilitan la obtención de mifepristona desde 2016 tuvieron menos consecuencias que su aprobación inicial del medicamento en 2000. Sería “difícil” argumentar que los cambios fueron “tan críticos para el público dado que la nación operaba, y se administró mifepristona a millones de mujeres, sin ellas durante dieciséis años”, escribieron los jueces.
Cuando el medicamento se aprobó inicialmente en 2000, la FDA limitó su uso hasta las siete semanas de embarazo. También requirió tres visitas presenciales al consultorio: la primera para administrar mifepristona, la siguiente para administrar el segundo fármaco misoprostol y la tercera para atender cualquier complicación. También requería la supervisión de un médico y un sistema de notificación de cualquier consecuencia grave asociada con la droga.
Esta semana, los ejecutivos farmacéuticos también firmaron una carta que condenaba el fallo de Texas y advertía que la aprobación de otros medicamentos por parte de la FDA podría estar en riesgo si se mantiene la decisión del juez federal de distrito Matthew Kacsmaryk.
En el centro de la demanda de Texas está la acusación de que la aprobación inicial de la mifepristona por parte de la FDA fue defectuosa porque la agencia no revisó adecuadamente los riesgos de seguridad.
La mifepristona ha sido utilizada por millones de mujeres durante los últimos 23 años. Si bien es menos drástico que anular por completo la aprobación del medicamento, el último fallo aún representa un gran desafío para la autoridad de la FDA que supervisa cómo se usan los medicamentos recetados en los EE. UU. El panel anuló varias decisiones tomadas por los reguladores de la FDA luego de años de revisión científica.
Los efectos secundarios comunes de los medicamentos con mifepristona incluyen calambres, sangrado, náuseas, dolor de cabeza y diarrea. En casos raros, las mujeres pueden experimentar un exceso de sangrado que requiere un procedimiento quirúrgico para detenerlo.
Más de 5,6 millones de mujeres en los EE. UU. habían usado el medicamento hasta junio de 2022, según la FDA. En ese período, la agencia recibió 4.200 informes de complicaciones en mujeres, o menos de una décima parte del 1% de las mujeres que tomaron el medicamento.